Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3) Zn+2HCl->ZnCl2+H2
a) \(n_{Zn}=\frac{13}{65}=0,2mol\)
Vì: \(\frac{0,2}{1}< \frac{0,5}{2}\)=> Zn hết, HCl dư.
\(n_{H_2}=n_{Zn}=0,2mol\)
\(V_{H_2}=0,2.22,4=4,48l\)
H=90%=> VH2 thu được là:4,032l
b) HCl dư: 0,5-(0,2.2)=0,1mol
mHCl=0,1.36,5=3,65g

Câu 1.
1. 4P + 5O2 → 2P2O5
2. 4H2 + Fe3O4 \(\underrightarrow{t^o}\) 3Fe + 4H2O
3. 3Ca + 2H3PO4 → Ca3(PO4)2 + 3H2
4. CaCO3 + 2HCl → CaCl2 + CO2 + H2O
5. Zn + 2HCl → ZnCl2 + H2\(\uparrow\)
6. Fe + CuSO4 → FeSO4 + Cu
7. CO2 + Ca(OH)2 → CaCO3 + H2O
các câu còn lại đọc lại sách hoặc là nghe những bài giảng trên mạng là sẽ làm đc, chứ tớ ngán làm quá

Đề 15:
1) Theo đề bài , ta có:
NTK(Y)= 2.NTK(Ca)= 2.40=80 (đvC)
=> Nguyên tố Y là brom, KHHH là Br.
2) - Đơn chất là chất do 1nguyên tố tạo thành.
VD: O3; Br2 ; Cl2;......
- Hợp chất là những chất do 2 hay nhiều nguyên tố hóa học trở lên tạo thành.
VD: NaCl, KMnO4, CuSO4, H2O;....
3) Khôi lượng mol? tự trả lời đi !
a) Khối lượng mol của phân tử gồm 2C và 4H
Có nghĩa là khối lượng mol của C2H4
\(M_{C_2H_4}\)= 2.12+4.1=28 (g/mol)
\(M_{H_2S}\)=2.1+32=34(g/mol)

\(a.d_{\dfrac{X_2}{O_2}}=2,218\\ m_{O_2}=32\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_{X_2}=32.2,218=71\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_X=\dfrac{71}{2}=35,5\left(\dfrac{g}{mol}\right)\\ \Rightarrow X.là.Clo\)
\(b.d_{\dfrac{Cl_2}{kk}}=\dfrac{71}{29}\approx2,4>1\\ \Rightarrow thu.bằng.pp.đặt.bình.đứng\)

- Khối lượng của CaO có trong chén sau khi nung là: 36,6 – 30 = 5,6(g)
- Số mol:
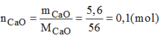
- Khối lượng khí C O 2 thoát ra sau phản ứng: 40 – 35,6 = 4,4(g)
- Số mol của khí C O 2 :
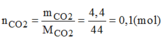
- Phân tử canxi cacbonat bị phân hủy thành CaO và C O 2 , có tỉ lệ số phân tử CaO:số phân tử C O 2 là 1:1.
a)
Ta có: NTK O = 16 đvC
Theo đề ta được:
\(\dfrac{M_O}{M_{Zn}}=\dfrac{16}{65,38}\)
\(\Leftrightarrow\dfrac{16}{M_{Zn}}=\dfrac{16}{65,38}\)
\(\Leftrightarrow M_{Zn}=65,38\)