Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

công thức oxit của sắt : Fe2Oy
nSO2=0,075 mol
2FexOy + (6x-2y)H2SO4 ---> xFe2(SO4)3 + (3x-2y)SO2 + (6x-2y)H2O
0,25 mol..........................................0,075 mol
theo pt trên ta có
\(\frac{0,25.2}{6x-2y}=\frac{0,075.2}{3x-2y}\)
<=> 0,75x-0,5y=0,45x-0,15y
<=>0,3x=0,35y<=> \(\frac{x}{y}=\frac{0,35}{0,3}=\frac{7}{6}\)
=> oxit sắt là Fe7O6
sao bạn lại để đấp án oxit fe như vậy làm j có công thức oxit fe đó

Đáp án:
8,625 g
Giải thích các bước giải:
nCl2=22,4/22,4=1 mol
nNaOH=0,1x2=0,2 mol
nCa(OH)2=0,1x0,5=0,05 mol
2NaOH+Cl2->NaCl+NaClO+H2O
0,2 0,1 0,1
2Ca(OH)2+2Cl2->CaCl2+Ca(ClO)2+2H2O
0,05 0,05 0,025
m=0,025x111+0,1x58,5=8,625 g

2KMnO4 + 16HCl ---> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
2Fe + 3Cl2 ---> 2FeCl3
Để điều chế đủ khí Clo thì số mol Cl2 = 3/2 số mol FeCl3 = 1,5.16,25/162,5 = 0,15 mol.
Số mol KMnO4 = 2/5 số mol Cl2 = 0,06 mol; m(KMnO4) = 0,06.158 = 9,48 g
V(HCl) = 0,48/1 = 480 ml.
KMnO4 + 16HCl ---> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
2Fe + 3Cl2 ---> 2FeCl3
Để điều chế đủ khí Clo thì số mol Cl2 = 3/2 số mol FeCl3 = 1,5.16,25/162,5 = 0,15 mol.
Số mol KMnO4 = 2/5 số mol Cl2 = 0,06 mol; m(KMnO4) = 0,06.158 = 9,48 g
V(HCl) = 0,48/1 = 480 ml.

nAg=0,01 mol
NaX+AgN03------->NaN03+AgX,áp dụng bảo toàn nguyên tố Ag,nAg sau=nAg truoc
0,01--------------------------------0,01
MNaX=1,03/0,01=103------------------->X=80------->Br

Đáp án C
Gọi công thức muối cần tìm là MX2.
Khi cho 150 gam dung dịch X tác dụng với dung dịch Na2CO3 dư có phản ứng:
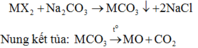
Do đó khí hấp thụ vào dung dịch KOH là CO2.
Vì sau phản ứng trong dung dịch vẫn còn KOH nên sản phẩm tạo thành là K2CO3:
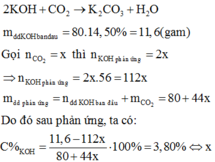 = 0,75
= 0,75

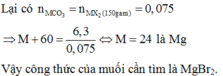



\(n_{NaOH}=2.0,3=0,6\left(mol\right)\)
\(PTHH:FeCl_x+xNaOH\rightarrow Fe\left(OH\right)_x+xNaCl\)
pt:__\(56+35,5x\left(g\right)\)__\(x\left(mol\right)\)_________________
pứ:____32,5(g)_____0,6(mol)__________________
Áp dụng định luật tỉ lệ:
\(\frac{56+35,5x}{32,5}=\frac{x}{0,6}\Rightarrow x=3\)
\(\rightarrow CTHH:FeCl_3\)