Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

bài 2 :
a) nhợp chất = V/22.4 = 1/22.4= 5/112 (mol)
=> Mhợp chất = m/n = 1.25 : 5/112 =28 (g)
b) CTHH dạng TQ là CxHy
Có %mC = (x . MC / Mhợp chất).100%= 85.7%
=> x .12 = 85.7% : 100% x 28=24
=> x=2
Có %mH = (y . MH/ Mhợp chất ) .100% = 14,3%
=> y.1=14.3% : 100% x 28=4
=> y =4
=> CTHH của hợp chất là C2H4
Bài 1.
- Những chất có thể thu bằng cách đẩy không khí là : Cl2,O2,CO2 do nó nặng hơn không khí
- Để thu được khí nặng hơn không khí ta đặt bình đứng vì khí đó nặng hơn sẽ chìm và đẩy không khí ra bên ngoài
- Đẻ thu được khí nhẹ hưn thì ta đặt bình úp vì khí đó nhẹ hơn cho nen nếu đặt đứng bình thì nó sẽ bay ra ngoài

a) PTHH: S + O2 =(nhiệt)=> SO2
b) nS = 3,2 / 32 = 0,1 (mol)
=> nO2 = nSO2 = nS = 0,1 (mol)
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VKK(đktc) = \(2,24\div\frac{1}{5}=11,2\left(l\right)\)

a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia phản ứng :
\(n_S=\frac{3,2}{32}=0,1\left(mol\right)\)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% về thể tích của không khí nên thể tích không khí cần dùng là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)
Bạn Đặng Quỳnh Ngân có thể giải thích cho mk tại sao Vkk=5.VO2
mk chưa hiểu đoạn đó cảm ơn bạn

a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia phản ứng :
\(n_S=\frac{3,2}{32}=0,1\left(mol\right)\)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
\(V_{SO_2}=22,4.0,1=2,24\left(l\right)\)
Tương tự thể tích khí oxi cần dùng ở đktc là :
\(V_{O_2}=22,4.0,1=2,24\left(l\right)\)
Vì khí oxi chiếm 20% thể tích của không khí nên thể tích không khí cần là :
\(V_{kk}=5.V_{O_2}=5.2,24=11,2\left(l\right)\)
Nếu thế số vào phương trình thì là :
Ta có phương trình hóa học :
S + O2 \(\rightarrow\) SO2
1mol 1mol 1mol
0,1 0,1 0,1

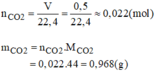
Mà C O 2 nặng gấp 1,5 lần không khí nên khối lượng không khí có trong cốc 0,5 lít ban đầu là:
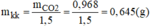
Vậy khi thay không khí bằng C O 2 thì khối lượng khí trong cốc tăng lên:
0,968 - 0,645 = 0,323(g)
Phải đặt thêm vào đĩa cân bên kia quả cân có khối lượng 0,323g để cân trở lại thăng bằng.

a) Số mol canxi cacbonat tham gia phản ứng
=
= 0,1 mol
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Theo phương trình hóa học, ta có:
=
= 0,1 mol
Khối lượng của canxi clotua tham gia phản ứng:
= 0,1 . (40 + 71) = 11,1 g
b) Số mol canxi cacbonat tham gia phản ứng:
=
= 0,05 mol
Theo phương trình hóa học, ta có:
=
= 0,05 mol
Thể tích khí CO2 ở điều kiện phòng là:
= 24 . 0,05 = 1,2 lít

Thể tích C O 2 thở ra trong 1 phút của 50 học sinh:
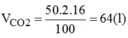
Trong 45 phút 50 học sinh này thở ra C O 2 :
64 x 45 = 2880(l) = 2,88( m 3 )
Bài 9 :
a , Vkk = 12 x 7 x 4 = 336 m3
Vì VO2 = \(\dfrac{1}{5}\cdot V_{kk}\Rightarrow V_{O2}=\dfrac{1}{5}\cdot336=67,2m^3\)
b, VCO2 của một học sinh thở ra một lần :
2 x 4% = 0,08 ( lít )
VCO2 của một học sinh thở ra trong 45 phút là :
0,08 x 16 x 45 = 57,6 lít
=> VCO2 của 50học sinh thở ra trong 45 phút :
57,6 x 50 = 2880 lít
Bài 11 :A. Mình chỉ nghĩ ra \(Mn_2O_7\) :V