Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án đúng: A
Giải chi tiết:
A chỉ chứa muối
B có H2SO4 là axit và Ba(OH)2 là bazo
C có HCl là axit
D có KOH là bazo còn nước không phải muối
Đáp án A
Dãy chất nào sau đây chỉ bao gồm muối:
A. MgCl2; Na2SO4; KNO2
B. Na2CO3; H2SO4; Ba(OH)2
C. CaSO4; HCl; MgCO3
D. H2O; Na3PO4; KOH
~HT~

a) Ta có : C = 12 đvC = 1,9926.10-23 (g)
=> 1 đvC = 1,9926.10−23121,9926.10−2312 ≈ 1,66.10-24 (g).
b) Khối lượng tính bằng gam của nguyên tử nhôm là :
mAl = 27 đvC = 27. 1,66.10-24 = 4,482.10-23 (g)
Đáp án C.

Fe+H2SO4-->FeSO4+H2
x---------------------x mol
Mg+H2SO4-->MgSO4+H2
y----------------------------y mol
nH2=\(\dfrac{8,96}{22,4}\)=0,4 mol
ta có hệ pt
56x+24y=16
x+y=0,4
==>x=0,2 mol, y=0,2 mol
=>%mFe=(\(\dfrac{0,2.56}{16}\).100=70%
=>%mMg=100-70=30%
=>m muoi=0,2.152+0,2.120=176,2g

a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
Bài giải:
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3

a) Ta có :
PTPU : Al + CuSO4 → Alx(SO4)y + Cu
Ta thấy :
Al có hóa trị III
So4 có hóa trị II
=> III . x = y . II
=> \(\dfrac{x}{y}=\dfrac{II}{III}=\dfrac{2}{3}\)
=> x = 2 ; y = 3
b) Ta có :
PTPU :
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Tỉ lệ cặp đơn chất là : 2 : 3
Tỉ lệ cặp hợp chất là : 3 : 1
a) PT: Al + CuSO4 -> Alx(SO4)y + Cu
ta có: Al (III) , SO4 (II)
=> III .x = y.II
vậy \(\dfrac{x}{y}=\dfrac{2}{3}\Rightarrow x=2;y=3\)
Nên công thức hóa học là \(Al_2\left(SO_4\right)_3\)
b) PTHH: 2Al + 3CuSO4 -> Al2(SO4)3 + 3Cu
2........3..................1.....................3
vậy tỉ lệ cặp đơn chất là Al và Cu là 2 : 3
tỉ lệ cặp hợp chất là CuSO4 và Al2(SO4)3 là 3 : 1
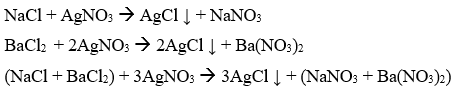
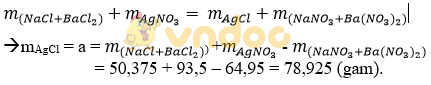

1)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ A_{Zn}=0,2.6.10^{23}=12.10^{23}\left(\text{nguyên tử}\right)\)
Để \(A_{Cu}=A_{Zn}\Rightarrow n_{Cu}=n_{Zn}=0,2\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
2)
A: SO3
B: H2O
C: H2SO4
D: Fe
E: FeSO4
F: CaO
G: H2
K: O2
\(SO_3+H_2O\rightarrow H_2SO_4\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ 2H_2+O_2\xrightarrow[]{t^o}2H_2O\\ CaO+H_2O\rightarrow Ca\left(OH\right)_2\)