Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

* Thí nghiệm 1: Cho hỗn hợp X tác dụng với dung dịch Br2
Đặt số mol anken A và ankin B lần lượt là x và y (mol)
nX = x + y = 0,5 (1)
CnH2n + Br2 → CnH2nBr2
x x
CmH2m-2 + 2Br2 → CmH2m-2Br4
y 2y
=> nBr2 = x + 2y = 0,8 (2)
Từ (1) và (2) ta có:
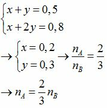
* Thí nghiệm 2: Đốt cháy hỗn hợp X
Hấp thụ CO2 vào dung dịch Ca(OH)2 thấy xuất hiện kết tủa, thêm KOH dư vào dung dịch thu được lại tiếp tục xuất hiện kết tủa nên ta có các phương trình hóa học sau:
CO2 + Ca(OH)2 → CaCO3 + H2O
0,25 ← 0,25
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 ← 0,025
Ca(HCO3)2 + 2KOH → K2CO3 + CaCO3 + 2H2O
0,025 ← 0,025
nCO2 = 0,25 + 0,05 = 0,3 mol
Ta có: m dung dịch giảm = mCaCO3 – mCO2 – mH2O => 7,48 = 25 – 0,3.44 – mH2O
=> mH2O = 4,32 gam => nH2O = 4,32/18 = 0,24 mol
Mặt khác, nB = nCO2 – nH2O = 0,3 – 0,24 = 0,06 mol
=> nA = 0,06(2/3) = 0,04 mol
BTNT C: nCO2 = n.nA + m.nB => 0,04n + 0,06m = 0,3
=> 2n + 3m = 15 (n≥2, m≥2)
| m |
2 |
3 |
4 |
| n |
4,5 |
3 |
1,5 |
Vậy A là C3H6 và B là C3H4
Khối lượng của hỗn hợp là: m = mC3H6 + mC3H4 = 0,04.42 + 0,06.40 = 4,08 (gam)


C2H4, C3H6, C4H8 cùng là anken nên có công thức chung là CnH2n
2CO + O2 → 2CO2↑ (1)
x → x (mol)
2H2 + O2 → 2H2O (2)
y → y (mol)
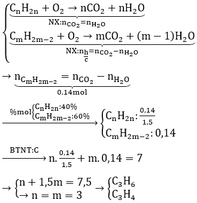
CnH2n + O2 → nCO2 + 2nH2O (3)
Sản phẩm cháy thu được gồm có CO2 và H2O.
Khi hấp thụ vào dd Ca(OH)2: 0,04 mol thu được dung dịch Y, thêm từ từ Ba(OH)2 vào dung dịch Y thu được kết tủa của các ion kim loại => CO2 phản ứng với Ca(OH)2 theo phương trình:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (4)
CO2 + Ca(OH)2 → Ca(HCO3)2 + H2O (5)
Dd Y chứa Ca(HCO3)2
BaCl2 + Ca(HCO3)2 → CaCO3↓ + BaCO3↓ + H2O (6)
m1 = mCaCO3(4)
m2 = mCaCO3(5) + mBaCO3
=> m1 + m2 = ∑ mCaCO3↓ + mBaCO3 = 6,955 (g) (*)
BTNT Ca: => ∑nCaCO3↓ = ∑ nCa(OH)2 (4+5) = 0,04 (mol)
Từ (*)

=> nCaCO3(6) = nBaCO3 = 0,015 (mol)
=> nCaCO3(4) = ∑nCa(OH)2 – nBaCO3 = 0,04 – 0,015 = 0,025 (mol)
BTNT C => ∑ nCO2 = ∑ nCaCO3 + nBaCO3 = 0,04 + 0,015 = 0,055 (mol)
Khối lượng dd Y tăng 0,82 gam so với dd Ca(OH)2 ban đầu
=> mCO2 + mH2O – mCaCO3(4) = 0,82
=> mH2O = 0,82 + 0,025.100 – 0,055.44 = 0,9 (g)
=> nH2O = 0,9 : 18 = 0,05 (mol)
BTKL ta có: mhhX + mO2 = mCO2 + mH2O
=> mO2 = 0,055.44 + 0,9 – 0,92 = 2,4 (g) => nO2 = 0,075 (mol)
BTNT O: nO( trong CO) + 2nO2 = 2nCO2 + nH2O
=> nO( trong CO) = 2.0,055 + 0,05 – 0,075.2 = 0,01 (mol) => nCO = 0,01 (mol)
Từ PTHH (1), (2), (3) ta thấy khi đốt cháy CnH2n luôn cho nH2O = nCO2 => sự chênh lệch mol CO2 và mol H2O là do đốt cháy CO và H2
=> nCO2 – nH2O = x – y = 0,055 – 0,05 = 0,005 (mol)
Mặt khác: nCO – nH2 = x – y = 0,005 (mol)
=> nH2 = nCO – 0,005= 0,01 – 0,005 = 0,055 (mol)
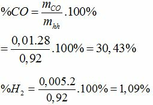

- Phần 1 tác dụng với Br2: nBr2 = 16:160 = 0,1 mol
C2H2 + 2Br2 → C2H2Br4
0,05 ← 0,1 (mol)
- Đặt số mol khí mỗi phần như sau:
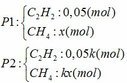
+ Số mol hỗn hợp khí X là: nX = 11,2:22,4 = 0,5 mol
Ta có: n khí P1 + n khí P2 = nX => 0,05 + x + 0,05k + kx = 0,5 <=> (x + 0,05)k = 0,45 - x
=> 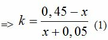
+ Đốt cháy phần 2:
C2H2 + 2,5O2 → t ∘ 2CO2 + H2O
0,05k → 0,1k→ 0,05k (mol)
CH4 + 2O2 → t ∘ CO2 + 2H2O
kx → kx → 2kx (mol)
Sản phẩm cháy gồm
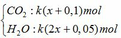
dẫn qua dung dịch Ba(OH)2 dư:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
k(x+0,1) → k(x+0,1) (mol)
Khối lượng dung dịch giảm: m dd giảm = mBaCO3 – mCO2 – mH2O
=> 197k(x+0,1) – 44k(x+0,1) – 18k(2x+0,05) = 69,525
=> 153k(x+0,1) – 18k(2x+0,05) = 69,525
=> k(117x+14,4) = 69,525
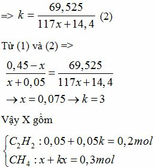
CaC2 + 2H2O → Ca(OH)2 + C2H2
0,2 ← 0,2 (mol)
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
0,1 ← 0,1 (mol)
Giá trị của m là: m = mCaC2 + mAl4C3 = 0,2.64 + 0,1.144 = 27,2 gam
Phần trăm thể tích các khí trong X là:

tác dụng với AgNO3 trong NH3 dư:
C2H2 + 2AgNO3 + 2NH3 → Ag2C2↓ + 2NH4NO3
0,15 → 0,15 (mol)
Khối lượng kết tủa thu được là: mAg2C2 = 0,15.240 = 36 gam

Câu 1 :
+ Dùng H2 khử MO :
MO + H2 -----------> M + H2O (1)
+ Theo đề bài : mH2SO4 ( trong dd 90%) = 15,3 . 90 /100 = 13,77 ( g)
+ Sau khi hấp thụ nước thì C% dd H2SO4 giảm xuống 86,34 %
=> mdd H2SO4 ( sau khi hấp thụ nước từ 1 ) = 13,77 . 100 % :86,34 % = 15,9485754 ( g)
=> m H2O được hấp thụ = 15,9485754 - 15,3 =0,6485754 (g)
=> n H2O được hấp thụ = 0,6485754 / 18 = 0,036
=> nH2O tạo ra ở (1) = 0,036 : 90% = 0,04 (mol)
=> nM = nMO (Pư) = 0,04 (mol )
+Hòa tan các chất rắn còn lại trong ống bằng dd HCl vừa đủ :
MgO + 2HCl ➜ MgCl2 + H2O (2)
Al2O3 + 6HCl ➜ 2AlCl3 + 3H2O (3)
=> dd B gồm : MgCl2 và AlCl3
Sau khi hòa tan, còn lại 2,56 gam M
=> MM = 2,56/0,04 = 64 ( Cu)
=> M là Cu
+ Lấy 1/10 dd B cho tác dụng với dd NaOH dư:
MgCl2 + NaOH ➜ Mg(OH)2 + NaCl (4)
AlCl3 + 3NaOH ➜ 3NaCl + Al(OH)3 (5)
Al(OH)3 + NaOH ➞ NaAlO2 + 2H2O (6)
+ Lọc kết tủa , nung đến khi khối lượng không đổi :
Mg(OH)2 ➜ MgO + H2O (7)
+ Thu được 0,28 g chất rắn
=> n MgO = 0,28 / 40 = 0,007 (mol )
+Theo (4)(7) :
1/10 nMgCl2 = 0,007 (mol)
=> n MgCl2 =0,007. 10 = 0,07 (mol)
+ Theo (2) :
n MgO = 0,07 (mol)
+ nCuO = 0,04 : 80% = 0,05 (mol)
=> %mMgO = 40 . 0,07 / 16,2 . 100% = 17,28 %
%mCuO = 80 . 0,05 /16,2 .100% = 24,69%
%mAl2O3= (16,2 - 0,05.64 - 0,07.40) / 16,2 .100% = 58,03%
P/S: mỏi tay quá @@

Khi cho NaOH dư vào thu thêm được kết tủa nên dung dịch có muối Ca(HCO3)2.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,5 ← 0,15
2CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + 2H2O
0,1 ← 0,1
→ nCO2 = 0,1.2 + 0,5 = 0,7
Mặt khác: mdd giảm = mCaCO3 – mCO2 + mH2O
→ 9,12 = 50 – (44.0,7 + 18.nH2O) → nH2O = 0,56

mdd giảm = m↓ - mCO2 → mCO2 = 10 - 3,4 = 6,6 gam → nCO2 = 6,6 : 44 = 0,15 mol.
C6H12O6 enzim−−−−→30−35oC→30-35oCenzim2C2H5OH + 2CO2
Theo phương trình: nC6H12O6 = 0,15 : 2 = 0,075 mol.
Mà H = 90% → nC6H12O6 = 0,075 : 90% = 1/12 mol → m = 180 x 1/12 = 15 gam

Đặt công thức A là CaHb
M tb của hỗn hợp:25,33.2=50,66
Số mol của hỗn hợp M là 3,36:22,4=0,15
-->Số mol của CaHb là 0,1; của CxH2x –2 là 0,05
Khối lượng của hỗn hợp là 50,66.0,15=7,6(g)
Đun sôi dung dịch không thấy có thêm kết tủa --> Vậy chỉ có phản ứng
Ca(OH)2+CO2-->CaCO3+H2O(1)
nCaCO3= số mol CO2=0,55-->mCO2=24,2 (g)
nC=0,55-->mC=12.0,55=6,6
-->mH=7,6-6,6=1
-->nH=1-->số mol H2O=0,5
PTTH CaHb + (a+b/4)O2 --> aCO2 + b/2H2O (2)
CxH2x–2+(3x -1)/2O2->xCO2 + (x-1)H2O (3)
Từ (2) và (3)
--> 0,1a + 0,05x = 0,55 (I)
--> 0,05b + 0,05 (x-1) = 0,5 (II)
Giải (I) và (II) 2a = b
Công thức HĐCB A có thể viết là CaH2a
Có 2 trường hợp xảy ra, khi 2 HĐCB khác nhau 1 nguyên tử C
+ TH1: CaH2a và C(a + 1)H 2(a+1) – 2
-->0,1a+0,05(a+1)=0,55
Giải ra a~3,33 Loại
+ TH2: CaH2a và C (a-1)H2(a-1) -2
-->0,1a + 0,05 (a-1) = 0,55
Giải ra a = 4 --> CTPT hai HĐCB là C4H8 và C3H4
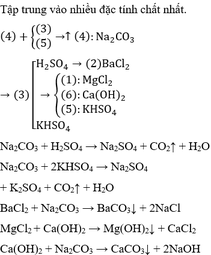
1.
CuO, khí CO2
BaSO4
CuO, khí CO2
BaSO4
6 tạo kết tủa vs 1, 2, 4 => 6 là K2CO3
1, 2 tạo kết tủa vs 3,6 => 1, 2 : Ba(NO3)2 , CaCl2 ; 3: Na2SO4
2+AgNO3 tạo kết tủa => 2: CaCl2 ; 1: Ba(NO3)2
5: CuCl2
Bạn tự viết pt nhé :> mình lười lắm T.T