Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: 3Fe + \(2O_2\) --->\(Fe_3O_4\)
theo pt: 3_____2_____________1
theo đề: x______y_____________0.01
nFe3O4 là: 0.01mol
\Rightarrow nO2= 0.01*2/1=0.02 mol
VO2= 0.02*22.4=0.448l
b, PTHH : 2KMnO4 ----> K2MnO4 + MnO2 + O2
theo pt: 2__________1________1______1
theo đề: x___________________________0.02
=> n KMnO4= 0.02*2/1= 0.04 mol
=>mKMnO4= 0.04*158=6.32g
a. số mol của Fe3O4 là :
2.32 : 232 =0.01 mol
theo tỉ lệ mol ta có số mol của Fe là:
0.01 * 3 = 0.03 mol
khối lượng sắt là: 0.03*56=1.68g
số mol oxi là: 0.01*2=0.02mol
thể tích oxi là: 0.02*22.4= 0.448g
b. 2KMnO_4 ---> K2MnO4 + MnO2 + O2
---> nKMnO_4 = 2nO2 = 0,04 mol ---> mKMnO_4=0.04*158=6.32g

Câu 5:
PTHH : H2+ Cl2 -to-> 2 HCl
Vì số mol , tỉ lệ thuận theo thể tích , nên ta có:
25/1 = 25/1 => P.ứ hết, không có chất dư, tính theo chất nào cũng được
=> V(HCl)= 2. V(H2)= 2. 25= 50(l)
Câu 4: mFe2O3= 0,6. 80= 48(g)
=> nFe2O3= 48/160=0,3(mol)
mCuO= 80-48=32(g) => nCuO=32/80=0,4(mol)
PTHH: CuO + CO -to-> Cu + CO2
0,4_______0,4_____0,4____0,4(mol)
Fe2O3 + 3 CO -to-> 2 Fe +3 CO2
0,3_____0,9____0,6______0,9(mol)
=>nCO= 0,4+ 0,9= 1,3(mol)
=> V(CO, đktc)= 1,3. 22,4=29,12(l)

a)\(n_{Fe_3O_4}=\dfrac{11,6}{232}=0,05mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,15 0,1 0,05
\(m_{Fe}=0,15\cdot56=8,4g\)
\(m_{O_2}=0,1\cdot32=3,2g\)
b)\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,2 0,1
\(m_{KMnO_4}=0,2\cdot158=31,6g\)
\(a,n_{Fe_3O_4}=\dfrac{11,6}{232}=0,05\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,15<--0,1<----------0,05
\(\rightarrow\left\{{}\begin{matrix}m_{Fe}=0,15.56=8,4\left(g\right)\\m_{O_2}=0,1.32=3,2\left(g\right)\end{matrix}\right.\)
b, PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,2<--------------------------------------0,1
=> mKMnO4 = 0,2.158 = 31,6 (g)

a.\(\%Fe=\dfrac{56.3}{56.3+16.4}.100=72,41\%\)
b.\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,04 0,02 ( mol )
\(m_{O_2}=0,04.32=1,28g\)
c.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,08 0,04 ( mol )
\(m_{KMnO_4}=0,08.158=12,64g\)

a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 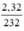 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.

\(n_{Fe_3O_4}=\dfrac{2.32}{232}=0.01\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{^{t^0}}Fe_3O_4\)
\(0.03......0.02.........0.01\)
\(m_{Fe}=0.03\cdot56=1.68\left(g\right)\)
\(m_{O_2}=0.02\cdot32=0.64\left(g\right)\)
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(0.04............................................0.02\)
\(m_{KMnO_4}=0.04\cdot158=6.32\left(g\right)\)
a)
n Fe3O4 = 2,32/232 = 0,01(mol)
3Fe + 2O2 \(\xrightarrow{t^o}\) Fe3O4
0,03....0,02.......0,01...........(mol)
m Fe = 0,03.56 = 1,68(gam)
m O2 = 0,02.32= 0,64(gam)
c)
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
n KMnO4 = 2n O2 = 0,04(mol)
m KMnO4 = 0,04.158 = 6,32 gam

a) Phương trình hóa học của phản ứng:
3Fe + 2O\(_2\) → Fe\(_3\)O\(_4\).
nFe3O4 = \(\dfrac{2,32}{232}\) = 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
a.
\(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,03 0,02 0,01 ( mol )
\(m_{Fe}=0,03.56=1,68g\)
\(m_{O_2}=0,02.32=0,64g\)
b.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,04 0,02 ( mol )
\(m_{KMnO_4}=0,04.158=6,32g\)

Bài 1:
\(a.PTHH:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\\ n_{Fe_3O_4}=\dfrac{m}{M}=0,3\left(mol\right)\)
Từ PTHH trên ta có:
3 mol sắt tác dụng với 2 mol khí oxi thì sinh ra 1 mol oxit sắt từ
=> 0,9 mol sắt tác dụng với 0,6 mol khí oxi thì sinh ra 0,3 mol oxit sắt từ
\(\Rightarrow m_{Fe}=0,9.56=50,4\left(g\right)\\ b.\Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\)
a) Ta có PTHH
2R + O2 \(\rightarrow\) 2RO
Theo ĐLBTKL : mR + mO2 = mRO
=> 7.2 + mO2 = 12
=> mO2 = 12 - 7.2 =4.8(g) => nO2 = m/M = 4.8/32 =0.15(mol)
Theo PT => nR = 2 . nO2 = 2 x 0.15 =0.3(mol)
=> MR = m/n = 7.2/0.3 =24(g)
=> R là Magie (Mg)
b)Ta có PTHH
2O2 + 3Fe\(\rightarrow\) Fe3O4 (1)
2KClO3 \(\rightarrow\) 2KCl + 3O2 (2)
nFe3O4 = m/M = 3.48/232=0.015(mol)
Theo PT(1) => nO2 = 2 . nFe3O4 = 2 x 0.015=0.03(mol)
=> VO2 = n x 22.4 = 0.03 x 22.4 =0.672(l)
Theo PT(1) => nFe = 3 . nFe3O4 = 3 x 0.015 =0.045(mol)
=> mFe = n .M = 0.045 x 56 =2.52(g)
Theo PT(2) => nKClO3 = 2/3 . nO2 = 2/3 x 0.03 =0.02(mol)
=> mKClO3 = n .M = 0.02 x 122.5 =2.45(g)
a) PTHH: 2R + O2 -to-> 2RO
Theo định luật bảo toàn khối lượng, ta có:
\(m_R+m_{O_2}=m_{RO}\\ =>m_{O_2}=m_{RO}-m_R=12-7,2=4,8\left(g\right)\)
=> \(n_{O_2}=\frac{4,8}{32}=0,15\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_R=2.n_{O_2}=2.0,15=0,3\left(mol\right)\)
=> \(M_R=\frac{7,2}{0,3}=24\left(\frac{g}{mol}\right)\)
Vậy: Nguyên tố R là magie (Mg=24).