Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2SO_4}=0,3.1=0,3\left(mol\right)\)
\(n_R=\frac{7,2}{M_R}\) (mol)
PTHH: \(R+H_2SO_4\rightarrow RSO_4+H_2\uparrow\)
______0,3<----0,3-------->0,3__________(mol)
=> \(\frac{7,2}{M_R}=0,3=>M_R=24\) (g/mol) => R là Mg
\(a=m_{MgSO_4}=0,3.120=36\left(g\right)\)

nHCl= 0,25 mol
\(\text{nH2SO4= 0,25.0,5= 0,125 mol}\)
\(\rightarrow\) nH+ = 0,5 mol
nH2=\(\frac{5,32}{22,4}\)= 0,2375 mol
\(\rightarrow\)\(\text{nH=0,2375.2= 0,475 mol}\)
Ta thấy nH < nH+ nên chỉ có 0,475 mol H+ đc nhận e, còn dư 0,025 mol H+
\(\rightarrow\)Axit dư

1. Trong 4 kim loại trên, không có kim loại nào tác dụng được với cả 4 dung dịch trên.
2. Chúng ta có thể dùng nước vôi trong để loại bỏ các khí độc trên là tốt nhất.
PTHH: Ca(OH)2 + 2H2S ===> 2H2O + Ca(HS)2
Ca(OH)2 + CO2 ===> CaCO3 + H2O
Ca(OH)2 + SO2 ===> CaSO3 + H2O
2Ca(OH)2 + 2Cl2 ===> CaCl2 + Ca(ClO)2 + 2H2O
3. Các cặp dung dịch không tác dụng được với nhau là:
+) Dung dịch HNO3 và dung dịch BaCl2
4. Những cặp chất sau đây tác dụng được với nhau là:
+) Al và dung dịch KOH

AgNO3 + HCl -> AgCl + HNO3
nAgCl=0,1(mol)
Theo PTHH ta có:
nHCl=nAgNO3=nAgCl=0,1(Mol)
C% dd HCl=\(\dfrac{36,5.0,1}{120}.100\%=3,42\%\)
mdd AgNO3=\(\dfrac{170.0,1}{10\%}=170\left(g\right)\)
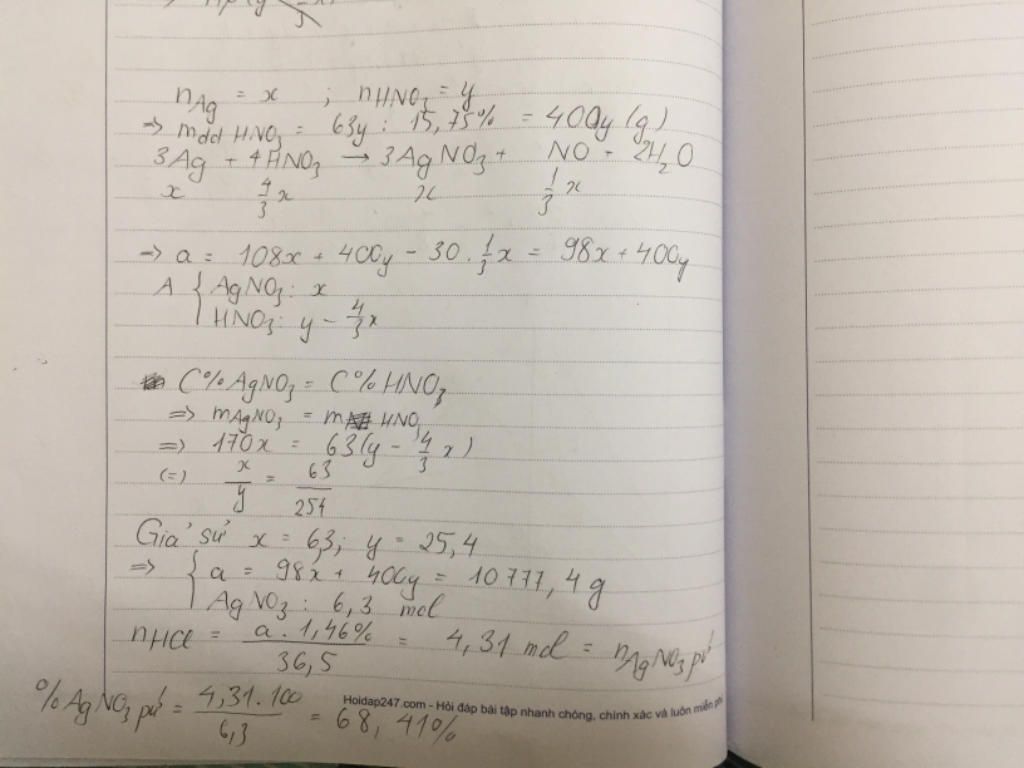
a) Đặt kim loại hóa trị II cần tìm là A.
\(n_{Ag}=\dfrac{75,6}{108}=0,7\left(mol\right)\\ A+2AgNO_3\rightarrow A\left(NO_3\right)_2+2Ag\\ n_A=\dfrac{n_{Ag}}{2}=\dfrac{0,7}{2}=0,35\left(mol\right)\\ M_A=\dfrac{m_A}{n_A}=\dfrac{19,6}{0,35}=56\left(\dfrac{g}{mol}\right)\)
Vậy kim loại A (II) cần tìm là sắt (Fe=56)
b)
\(n_{AgNO_3}=n_{Ag}=0,7\left(mol\right)\\ C_{MddAgNO_3}=\dfrac{0,7}{0,14}=5\left(M\right)\)
c)
\(V_{ddsau}=V_{ddAgNO_3}=0,14\left(l\right)\\ C_{MddFe\left(NO_3\right)_2}=\dfrac{0,35}{0,14}=2,5\left(M\right)\)