Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
Các phản ứng đã xảy ra có thể sơ đồ hóa thành:
Ankan -> Ankan’ + Anken
Dựa vào hệ số cân bằng của phản ứng crackinh, ta thấy : Thể tích (hay số mol) khí tăng sau khi phản ứng đúng bằng thể tích (hay số mol) ankan đã tham gia crackinh.
Ở đây là: V = 1010 – 560 = 450 lít
Do đó, phần C4H10 chưa bị crackinh là 110 lít

Giả sử: VC4H10 (pư) = x (l)
⇒ V hhkhí tạo thành = 2x (l) và VC4H10 (còn lại) = 560 - x (l)
⇒ 2x + 560 - x = 1010
⇒ x = 450 (l)
⇒ VC4H10 (chưa cracking) = 560 - 450 = 110 (l)
Bạn tham khảo nhé!

PTHH: \(C_4H_{10}\xrightarrow[]{cracking}C_aH_{2a+2}+C_bH_{2b}\left(a+b=4;a,b\in N;a\ge1;b\ge2\right)\)
Cứ mỗi 1 mol C4H10 pư sẽ tạo ra 2 mol sản phẩm => tăng 1 mol => mol tăng cũng là mol C4H10 pư
Ta có:
\(\Delta n_{\uparrow}=n_{C_4H_{10}\left(p\text{ư}\right)}=540-300=240\left(mol\right)\\ \Rightarrow H=\dfrac{240}{300}.100\%=80\%\)

Đáp án B
Crackinh C4H10 → hhX gồm 6 hiđrocacbon và H2 có V = 30 lít.
Dẫn hhX vào dd nước Br2 dư có 20 lít khí thoát ra.
20 lít khí thoát ra gồm CH4, C2H6, C3H8, C4H10 dư và H2 cũng chính là thể tích C4H10 ban đầu
→ VC4H10ban đầu = 20 lít.
VC4H10phản ứng = 30 - 10 = 10 lít
⇒ H = 10 20 = 50 %

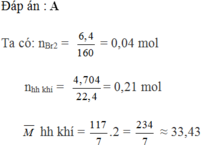
Khi dẫn hỗn hợp A gồm các hidrocacbon qua dung dịch brom, brom bị mất màu hết => anken trong hỗn hợp A có thể còn dư.
Ta thấy: hh khí = 33,43 < MC3H6 = 42
=> khí đi ra khỏi dung dịch brom có C3H6 => nC3H6 phản ứng = nBr2 = 0,04 mol
Áp dụng định luật bảo toàn khối lượng ta có:
mC4H10 = mC3H6 phản ứng + mhh khí = 0,04.42 + 0,221.234/7 = 8,7 (g)

GS : nA = 1 (mol)
=> nA (pư) = 0.6 (mol)
nA (dư) = 0.4 (mol)
\(C_nH_{2n+2}\underrightarrow{t^0,xt}C_aH_{2a}+C_bH_{2b+2}\left(n=a+b\right)\)
\(M_B=2\cdot18.125=36.25\left(\dfrac{g}{mol}\right)\)
\(m_B=36.25\cdot\left(0.6\cdot2+0.4\right)=58\left(g\right)\)
\(BTKL:m_A=m_B=58\left(g\right)\)
\(M_A=14n+2=58\left(\dfrac{g}{mol}\right)\Rightarrow n=4\)
\(C_4H_{10}\)

Đáp án B
Crackinh 0,2 mol C4H10 → hhX gồm 5 hiđrocacbon.
hhX qua bình Brom dư → mbình tăng = 8,4 gam
• Khí bay ra khỏi dung dịch Brom là hiđrocacbon no CT
→ nY = 0,2 mol, mhhY = 0,2 x 58 - 8,4 = 3,2 gam.
→ M = 16 → n = 1
![]()
→ VO2 = 22,4 x 0,4 = 8,96 lít

Đáp án A
hhX gồm H2 và CxHy
Nung nóng 0,85 mol hhX có xtNi
→ 25,2 gam hhY gồm các hiđrocacbon; dY/H2 = 21.
• Ta có ∑nY = 25,2 : 42 = 0,6 mol
→ nH2 = nX - nY = 0,85 - 0,6 = 0,25 mol
→ mH2 = 0,25 x 2 = 0,5 gam
\(C_4H_{10} \to C_2H_6 + C_2H_4\\ C_4H_{10} \to CH_4 + C_3H_6\\ C_4H_{10} \to C_4H_{10\ dư}\)
Theo PTHH, ta thấy :
\(2V_{C_4H_{10}\ pư} + V_{C_4H_{10}\ dư} = 1010\\ V_{C_4H_{10}\ pư} + V_{C_4H_{10}\ dư} = 560\\ \Rightarrow V_{C_4H_{10}\ pư} = 450 ; V_{C_4H_{10}\ dư} = 110\\ H = \dfrac{450}{560}.100\% = 80,36\%\)
Bn ơi mk ko hiểu lắm bài giải của bạn nơi ạ bạn có thể lý giải cho mk cái pt đc ko