Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1/ Gọi CT: MxOy
%O = 100 - 63.218 = 36.782 (%)
Theo đề bài ta có: Mx/63.218 = 16y/36.782
=> 36.782Mx = 1011.488y
=> Mx = 27.5y => M = 27.5y/x
Nếu x = 1, y = 1 => M = 27.5 (loại)
Nếu x = 2, y = 1 => M = 55 (Mn)
Nếu x = 3, y = 1 => Loại
Vậy CT: MnO2

Gọi CTHH của oxit là $Fe_xO_y$
Ta có :
$\%Fe = \dfrac{56x}{56x + 16y}.100\% = 72,41\%$
$\Rightarrow \dfrac{x}{y} = \dfrac{3}{4}$
Với x = 3 ; y = 4 thì thỏa mãn
Vậy oxit là $Fe_3O_4$

nFe = 5,6/56 = 0,1 (mol)
=> nFe2O3 = 0,1/2 = 0,05 (mol)
mFe2O3 = 0,05 . 160 = 8 (g)
=> C

Đặt công thức phân tử của oxit sắt là F e x O y (sắt có hóa trị 2x/y)
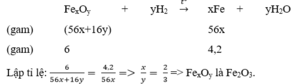

nFe=0,1mol
2Fe2O3+6H2 -> 4Fe+6H2O ( đk nhiệt)
0,05 <- 0,1
mFe2O3=0,05.(56.2+16.3)=8g

a)
$m_{Fe_2O_3} = 1000.90\% = 900(kg)$
$n_{Fe_2O_3} = \dfrac{900}{160} = 5,625(kmol)$
$n_{Fe} = 2n_{Fe_2O_3} = 11,25(kmol)$
$m_{Fe} = 11,25.56 = 630(kg)$
b)
$n_{Fe} = \dfrac{1000}{56}(kmol)$
$n_{Fe_2O_3} = 0,5n_{Fe} = \dfrac{125}{14}(kmol)$
$m_{Fe_2O_3} = \dfrac{125}{14}.160 = \dfrac{10000}{7}(kg)$
$m_{quặng} = \dfrac{10000}{7} : 90\% = 1587,3(kg)$
1. Gọi CT của oxit sắt là \(Fe_xO_{_{ }y}\)
Ta có : %O = 100%-72,41%=27,59.
\(\dfrac{\%Fe}{\%O}=\dfrac{72,41}{27,59}\) => \(\dfrac{56x}{16y}=\dfrac{72,41}{27,59}\)
=> \(\dfrac{x}{y}=\dfrac{3}{4}\)
Vậy công thức của oxit sắt là Fe3O4
2. Đặt CTTQ là MxOy
Ta có \(\dfrac{\%M}{\%O}=\dfrac{Mx}{16y}=\dfrac{63,218}{100-63,218}\)
=> \(M=27,5\times\dfrac{y}{x}=13,75\times\dfrac{2y}{x}\)
Ta có bảng biện luận:
Với \(\dfrac{2y}{x}\)là hóa trị của M. Chọn \(\dfrac{2y}{x}=4\) và M= 55
=> M là Mn
Vậy công thức của oxit là MnO2