Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a)n_{Ba\left(OH\right)_2}=0,05\cdot0,2\cdot2=0,02mol\\ pH=1\Rightarrow\left[OH^-\right]=0,1M\Rightarrow n_{HCl}=0,1\cdot0,3=0,03mol\\ n_{Ba\left(OH\right)_2}+n_{HCl}=0,02+0,03=0,05mol\\ \Rightarrow C_M=\dfrac{0,05}{0,5}=0,1M\Rightarrow pH=1\)

* M có hóa trị k đổi
=> BT nguyên tố M: nM/muối=nM/oxit
<=> \(\dfrac{5,6}{M+60}=\dfrac{4}{M+16}\)
=> M=94
=> k có kl nào thỏa mãn
mình làm M có htri thay đổi cũng k ra chắc đề bài sai đâu đó bạn kt lại nhé
2) nco2=0,3 mol
n OH-=0,35 mol
1<nOH-/nCO2=0,35/0,3<2
=> tạo 2 muối
pt ion: OH- + CO2 -> HCO3-
nHCO3- tính theo nCO2=0,3 mol
HCO3 + OH- -> CO32-+ H2O
nCO32-tính theo nOH- vì nOH- còn lại =0,05<nHCO3-
=> nCO32-=0,05 mol
nCa2+=0,1 mol > nCO32-
=> n kết tủa=n co32-=0,05 mol
=> m kết tủa=5g
Bài 2 :
1 < T = \(\dfrac{n OH-}{n CO3 2-}\)= \(\dfrac{0,35}{0,3}\) < 2
-> Tạo 2 muối
nkết tủa = nOH- -nCO2 = 0.35 - 0.3 = 0.05 (mol)
-> mkết tủa = 5 (gam)

nCO2=\(\frac{4,48}{22,4}\)=0,2(mol)
Ta có \(\frac{nCa\left(OH\right)2}{nCO2}\)= 0,75<1
\(\rightarrow\) Tạo 2 muối
Ca(OH)2 + CO2\(\rightarrow\)CaCO3 +H2O
0,15______0,15___0,15
CaCO3 + CO2 + H2O\(\rightarrow\) Ca(HCO3)2
0,05___0,05____________0,05
m muối=0,05.162+0,1.100=18,1(g)

1. nCa(OH)2=15*0,01=0,15 mol
Khi sục khí CO2 vào thì kết tủa xuất hiện:
CO2 + Ca(OH)2 -> CaCO3 + H20
Ta có: nCO2 : nCa(OH)2 = 1:1
Mà: 0,02 <= n CO2 <= 0,17 nên CO2 dư,kết tủa bị hòa tan
CaCO3 +H20 + CO2 -> Ca(HCO3)2 (tan)
Tỉ lệ là 1:1 nên kết tủa thu được nhiều nhất khi nCO2=nCa(OH)2=0,15 mol => mCaCO3=15g
* Xét khoảng 0,02 <= n CO2 <= 0,15, lúc này số mol CO2 càng tăng thì khối lượng kết tủa càng lớn => Khối lượng kết tủa nhỏ nhất khi nCO2 = 0,02 mol => mCaCO3=0,02* 100 = 2g
* Xét khoảng 0,15 < n CO2 <= 0,17, lúc này số mol CO2 càng tăng thì khối lượng kết tủa càng giảm=> nCO2 có thể dư nhiều nhất là 0,17 - 0,15=0,02 mol => nCaCO3 bị hòa tan = nCO2 =0,02
=> mCaCO3 thu được khi nCO2= 0,17 mol là: 0,15 - 0,02*100 = 13g
Vậy khối lượng kết tủa thu được trong khoảng [2;15]g
Chúc bạn học tốt!

CO2 + Ca(OH)2 → CaCO3 + H2O
0,1 0,1 0,1
2CO2 + CaCO3 + H2O → Ca(HCO3)2
0,16 – 0,1 → 0,06
=> n↓= 0,04 mol
n↓= 0,04 mol => m ↓ = 4g < 0,16 . 44 = 7,04g
=> mdd tăng = 7,04 – 4 = 3,04g
nCa(OH)2 = 2.0,05=0,1(mol)
ta có nCO2/nCa(OH)2 = 0,16/0,1 = 1,6
=> có 2 phản ứng xảy ra
CO2 + Ca(OH)2 ---> CaCO3 + H2O (1)
2CO2 +Ca(OH)2 ---> Ca(HCO3)2 (2)
bảo toàn C ta có x +2y = 0,16(3)
bảo toàn Ca ta có x +y = 0,1 (4)
từ (3) và (4) => x= 0,04(mol) y= 0,06(mol)
mCa(HCO3) = 0,06.145= 8,7(g)
m Ca(OH)2 = 0,1.57 = 5,7g
vậy khối lượng của Ca(HCO3)2 tăng 3g so với Ca(OH)2 ban đầu

H3PO4 + K2HPO4 →2KH2PO4
H3PO4 + Ca(OH)2 →CaHPO4 +2H2O
2H3PO4 + 3Ca(OH)2 →Ca3(PO4)2 +6H2O
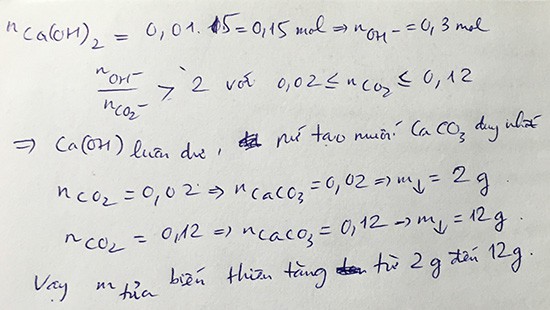
\(n_{CaCO_3}=\dfrac{10}{100}=0.1\left(mol\right)\)
\(TH1:\)
\(n_{CO_2}=n_{CaCO_3}=0.1\left(mol\right)\)
\(V=0.1\cdot22.4=2.24\left(l\right)\)
\(TH2:\)
\(n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=0.1+2\cdot\left(0.15-0.1\right)=0.2\left(mol\right)\)
\(V=0.2\cdot22.4=4.48\left(l\right)\)
\(\Rightarrow2.24\left(l\right)< V< 4.48\left(l\right)\)
\(V_{CO_2}=2,24\left(l\right)\) cũng được mà a nhỉ ??